
前言
随着靶向治疗药物的发展,越来越多的偶联药物展现出优异的临床效果,泛偶联时代的巨幕已经悄然拉开。抗体偶联药物(ADC)、多肽偶联药物(PDC)、小分子偶联药物(SMDC)、抗体片段偶联药物(FDC)、免疫刺激抗体偶联药物(ISAC)、放射性核素偶联药物(RDC)、病毒样药物偶联物(VDC)、抗体-siRNA偶联物(ARC)、抗体细胞偶联药物(ACC)等,让人们相信“万物皆可偶联”不再停留于假想阶段。由于ADC优异的表现,据不完全统计,每100款在研的偶联药物,其中41款属于ADC,可见ADC在偶联药物中的地位。本文将介绍ADC的特点,并探讨如何借助工程技术实现ADC安全、高效的生产,让“魔法子弹”魔力倍增。
ADC的发展历程
早在1913年,德国科学家Paul Ehrlich就提出了魔法子弹(“magic bullet”)的概念,其基本设想是将毒素选择性的输送到肿瘤部位。但是受到当时技术水平的限制,这个概念还仅存在于假设阶段。直到1958年,才有人开始细胞水平的研究。1975年,ADC开始用于动物模型的研究。1983年,ADC开始应用于临床试验。2000年,FDA加速批准了全球第一款ADC(商品名为Mylotarg)上市。然而Mylotarg由于明显的副作用,不得不于2010年退市。2011年全球第2款ADC(商品名为Adcetris)通过了FDA的上市审批,至此距离ADC概念的提出已接近1个世纪。直到2018年底,全球上市的ADC仅有5款。随后的几年,得益于抗体技术的成熟,2019年至2022年,ADC的商业化迎来一股热潮。截至2022年6月,已经上市的ADC达到了14款,分别是Adcetris®、Kadcyla®、Besponsa®、Mylotarg®,Polivy®、Padcev®、Enhertu®、Trodvy®、Blenrep®和Zynlonta™、Lumoxiti、Akalux、爱地希®、Tivdak。根据发表在 Nature Reviews 的《The oncology market for antibody-drug conjugate 》(Carolina do Pazo 等)一文,最早上市的 10 款 ADC 药物市场规模预计到 2026 年将超过 164 亿美元。
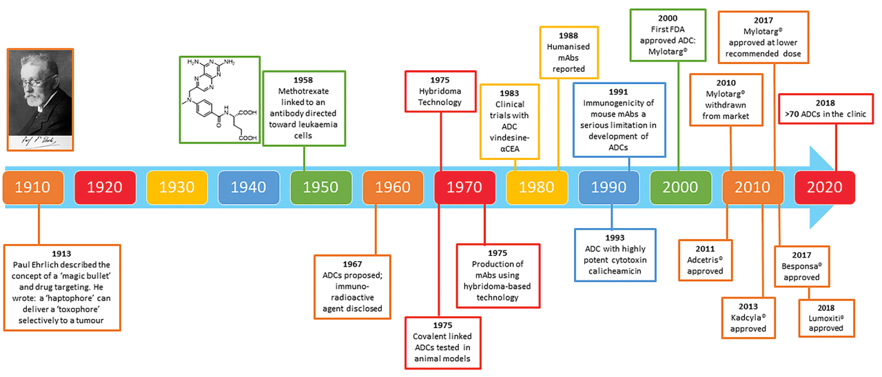
图片来源:Cytotoxic Payloads for Antibody–Drug Conjugates
在100多年的发展历程中,ADC经历了三代技术的更迭。早期的ADC,由于技术不成熟,药效差、毒副作用强、治疗窗狭窄,属于第一代ADC,代表产品为Mylotarg。随着抗体技术的成熟以及偶联技术和连接子的改良,第二代ADC的药效有了提升,毒副作用减小、治疗窗口更宽,但是依然存在偶联药物分布随机的问题,代表产品为Adcetris、Kadcyla等。为了进一步提高药效、降低毒副作用,采用定点偶联技术和新型细胞毒素的第三代ADC应运而生,代表产品为Enhertu、Trodvy。

ADC的结构及作用机理
ADC在100多年的发展历程中,目前只有14款药物成功上市,其开发难点不言而喻。接下来我们了解一下ADC的结构组成和作用机理。
ADC 药物通常包含下述三个关键组成部分:抗体(Antibody)、连接子(Linker)、小分子细胞毒性药物(Payload)。这三部分并称为ADC的三要素,如图所示。关于ADC三要素及偶联技术的内容,将在其他文章中进行介绍。
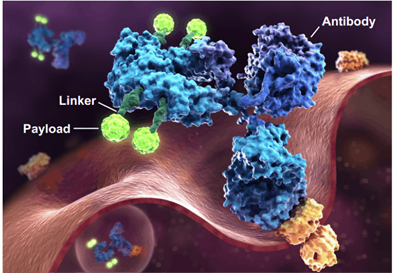
ADC三要素,图片来源:ADC REVIEW
进入血液的ADC 如何发挥作用呢?可以概括为6个步骤:
01. ADC的抗体成分可以识别肿瘤细胞表面的抗原并结合
02. ADC-抗原复合物通过内吞作用进入肿瘤细胞
03. ADC-抗原复合物进入溶酶体,抗体部分在溶酶体内降解
04. 细胞毒性药物从溶酶体中释放出来
05. 细胞毒性药物破坏 DNA 或维管束,以抑制肿瘤细胞的生长和分裂
06. 肿瘤细胞死亡
具有旁观者效应的ADC,在完成上述作用后,还可以继续攻击其他肿瘤细胞。
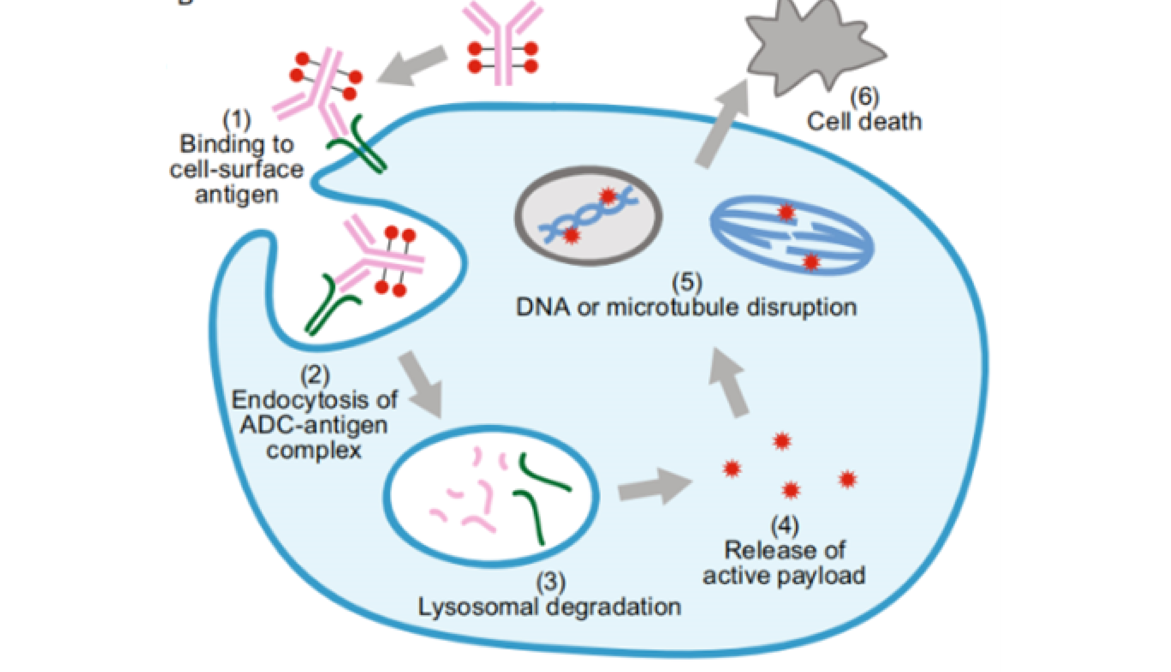
图片来源:Protein Cell 2018, 9(1):33-46
ADC生产难点及解决方案
01 生产路线及原辅料复杂
ADC是一种三元复合物形成的单一分子。ADC的生产涉及抗体的生产、毒性药物及连接子的生产、偶联物的生产、制剂生产等四个部分,如下图所示。这四个部分要求不同,对于生产设施、空调系统及公用工程系统、物料管理等,都是不小的挑战。对于一个制药企业来讲,生产的难度和成本都比普通的大分子或者小分子要大得多。因此,有些企业选择将ADC产品多产地生产,或者将一部分工段委托CMO企业生产。由此带来的合规性和供应链管理也是ADC药物生产的一大挑战。
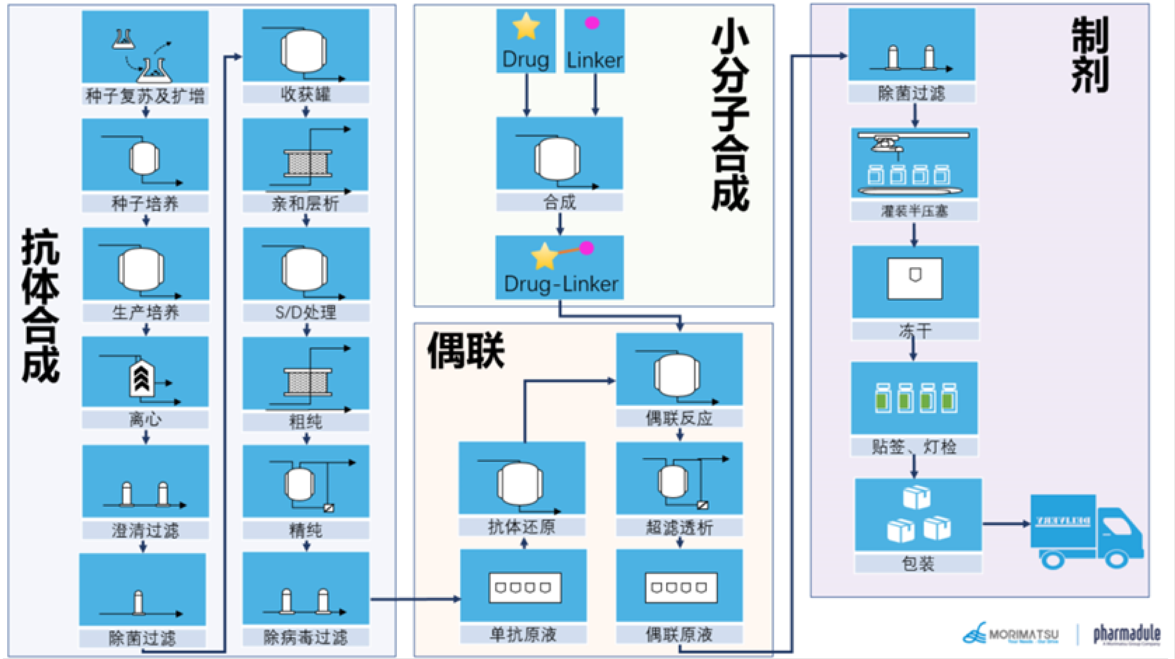
图片来源:典型ADC生产流程
02 药物毒性造成的安全风险
ADC所使用的细胞毒性药物,按照美国国家职业安全卫生研究所NIOSH的要求,其对应的职业暴露等级(Occupational Exposure Band ,OEB)为OEB4或OEB5的,需要使用隔离器。
中国国家药品监督管理局发布的《抗体类药品现场检查指南(征求意见稿)》,将有毒有害固体和液体OEB分为6个等级。OEB等级为4级及以上的固体物质应在隔离器中操作;含有OEB等级为4级及以上物料的液体的相关操作应在密闭容器/系统中进行。从安全防护及无菌保障的角度考虑,ADC制剂生产首选在隔离器中进行。应根据OEB等级选择合适的防护装置用于接触ADC制品的人员保护,人员着装应最大程度的减少身体暴露(如果采用隔离器技术,应关注隔离器的密闭性、使用前后手套完整性检测;隔离器回风管路定期清洗,应考虑隔离器内部设有清洗装置,生产结束进行隔离器内部清洗完毕后再打开隔离器门),处理制品暴露的人员需进行定期培训及考核。
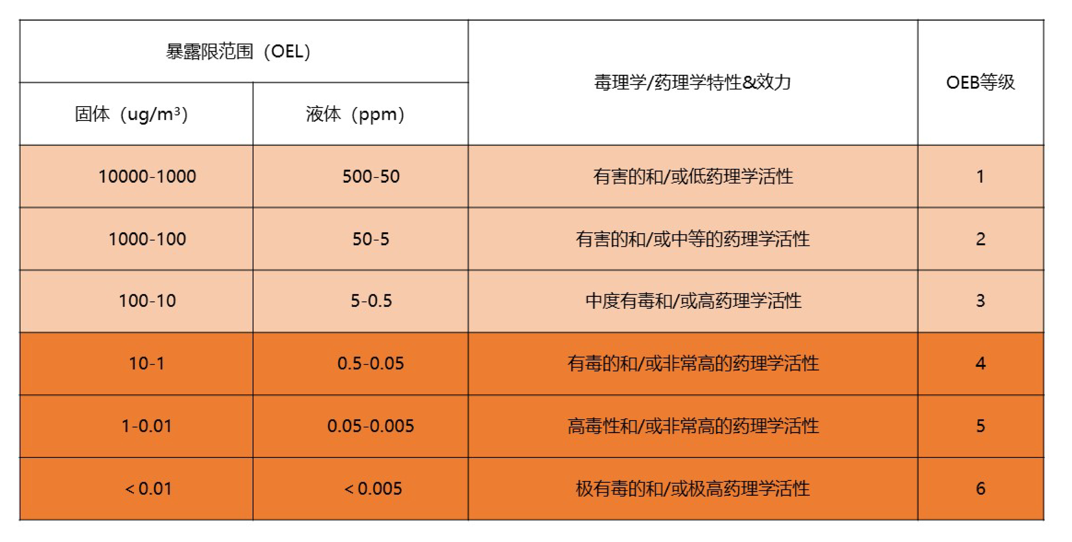
表 《抗体类药品现场检查指南(征求意见稿)》OEB及OEL指导
03 产品质量属性的控制
由于ADC兼具有抗体和小分子细胞毒性药物的生产工段。每个工段都有其独特的关键质量属性。抗体生产工段和小分子细胞毒素的质量属性应分别符合抗体药物生产的质量属性和小分子药物生产的质量属性。除此以外,ADC与其他大分子生物药物不同,ADC 药物具有独特的异质性,不同DAR 值(Drug-to-Antibody Ratio)的ADC 药物将会体现不同的药物临床效果。应根据对ADC 药物关键质量属性的影响确定关键工艺参数/步骤和工艺参数范围,并随着对产品和工艺的更深理解及生产经验的积累,确定生产过程中的中间体、粗品及终产品的质量控制策略,确保生产批间一致性,从而保证ADC 药物的安全、有效、质量可控。ADC的关键质量属性包括但不限于:药物抗体偶联比(DAR)、药物分布比例(偶联位点)、游离小分子药物、分子大小变异体(多聚体或片段)、残留溶剂等。
04 产品收率
根据ADC生产过程中使用的偶联技术不同,可以将偶联技术分为随机偶联技术和定点偶联技术。无论使用哪种偶联技术,在生产过程中,都可能出现未偶联、偶联位点错误、偶联数量错误、二聚体或多聚体等副产物,这些都会导致目标产物的收率降低。为了控制产品收率,采用合适的偶联技术、恰当的抗体修饰、优化偶联反应条件等,将有利于提高目标产物的收率。
基于对产品工艺的深入理解和行业法规的准确解读,森松可以为ADC的研发、中试及商业生产提供含核心设备(Machine)、增值服务(Value-added)、模块化工程(Plant)在内的数智化整体工程解决方案。森松特有的全生命周期的服务覆盖从联合研发、工艺放大、可行性研究、基础设计、概念设计、数字化顶层设计等前端服务,到产品生产,以及交付后的数字化运维、验证等后端服务,更好帮助药企快速实现工艺转移、工艺放大和产业化生产。
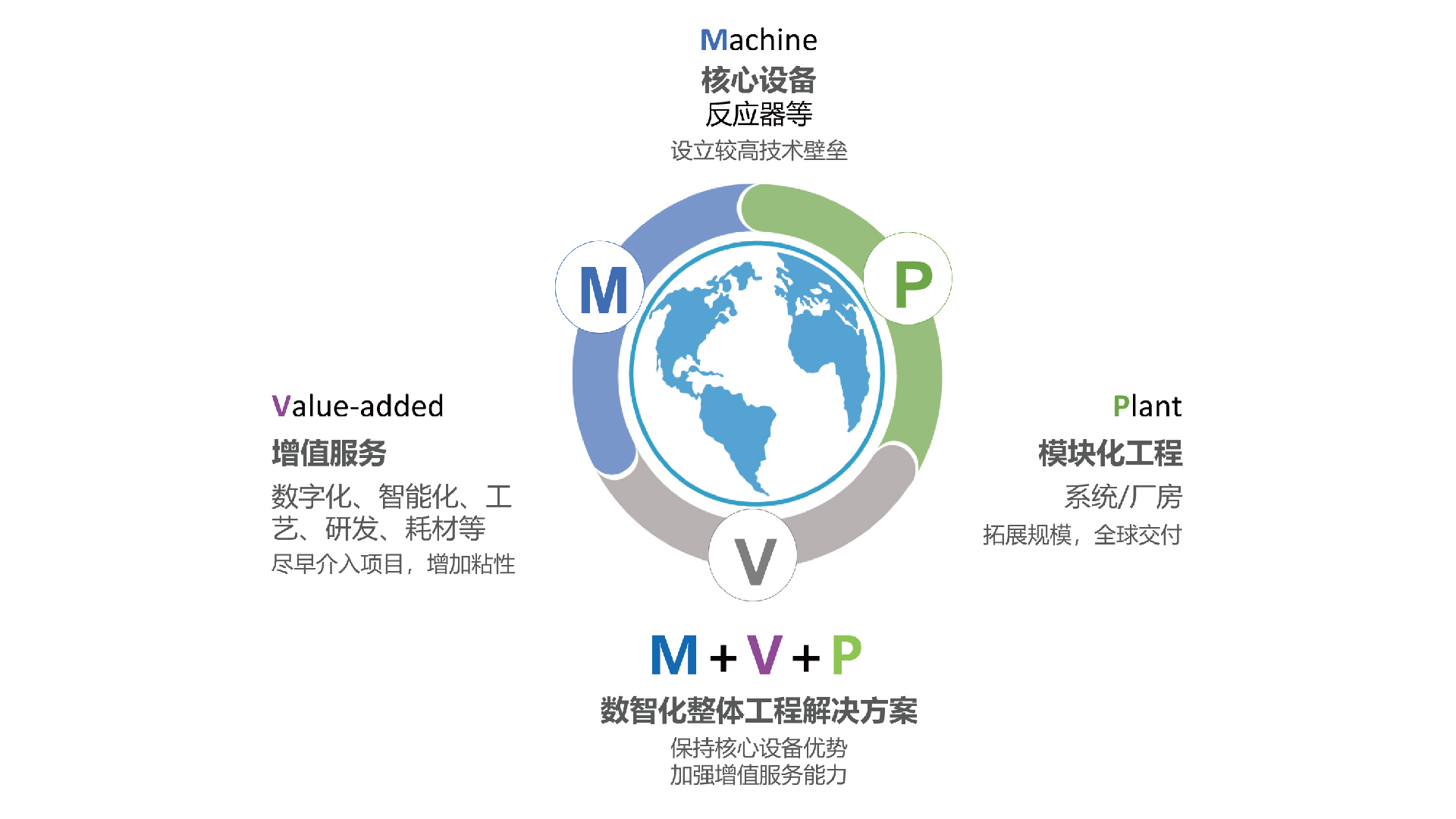

在ADC的抗体制备、小分子生产、偶联生产阶段,森松可提供的核心设备和模块化系统如下:
抗体制备
生物反应器、培养基配储系统、缓冲液配储系统、在线配液系统、分离和收获系统、纯化系统、浓缩及分装系统、生物废水灭活系统等。
小分子生产
反应釜、温控系统等。
ADC偶联生产
桌面反应器、不锈钢反应釜、一次性配储液袋、配液系统、超滤系统、隔离器等,以及制剂需要的配液及除菌过滤系统等。

除此以外,为了帮助药企加速产品上市,森松的模块化工厂可以节约新建厂房的建造时间并大幅度降低建造过程的风险,同时可以实现建筑的整体异地搬迁,让您的研发中心和生产基地插上“翅膀”,哪里需要就飞到哪里。
选择与森松合作,让您的“魔法子弹”ADC的魔力倍增!
关于上海森松制药设备工程有限公司
上海森松制药设备工程有限公司是森松国际控股有限公司(股票代码:2155.HK)的附属公司。森松源于日本,立足中国,布局全球,现已发展成为在核心设备、工艺系统、数智化工程解决方案等领域掌握核心技术并具有丰富项目经验的多元化跨国公司。依托在中国的先进制造基地,公司在瑞典、美国、印度、意大利等地开设了附属公司,并依靠其全球化的高效专业团队,截至目前已向40多个国家和地区交付了不同形式的产品和服务。
前瞻性声明
本新闻稿所发布的信息中可能会包含某些前瞻性表述。这些表述本质上具有相当风险和不确定性。在使用“预期”、“相信”、“预测”、“期望”、“打算”及其他类似词语进行表述时,凡与本公司有关的,目的均是要指明其属前瞻性表述。本公司并无义务不断地更新这些预测性陈述。
这些前瞻性表述乃基于本公司管理层在做出表述时对未来事务的现有看法、假设、期望、估计、预测和理解。这些表述并非对未来发展的保证,会受到风险、不确性及其他因素的影响,有些乃超出本公司的控制范围,难以预计。因此,受我们的业务、竞争环境、政治、经济、法律和社会情况的未来变化及发展的影响,实际结果可能会与前瞻性表述所含资料有较大差别。